源可定位机理概述
源可定位是指神经调控诱发的皮层活动在空间上与物理刺激靶区高度一致,并通过 EEG 源成像(dSPM)客观验证。本文中,靶区 ROI 由超声换能器放置位置(电极 C1、C3、FC1、FC3 之间的空隙,图1B)正交投影至皮层定义。实现源可定位需同时具备三个要素:一是存在空间特异性的亚阈值调节能力(毫米级);二是存在持续的、非时间锁定的膜电位基线偏移,将亚阈值信号“放大”为超阈值输出;三是避免来自非靶区(如听觉通路)的超阈值响应掩盖靶区信号。验证方法包括传感器层面的置换聚类检验(比较同侧与对侧 ROI 电极在 0–200 ms 窗口的差异,图2B)和源层面的 dSPM 活动对比(图3B),并通过最高活动点与 ROI 的欧氏距离量化空间精度。

图1 实验方法与刺激参数示意
图1展示了本研究的整体实验设计与技术参数。
图1A为实验范式示意图:受试者在闭眼静息状态下接受三种刺激条件——单独 tFUS、单独 HD‑tDCS(含空间对照超声)、以及 tEAS(tFUS 与 HD‑tDCS 同时施加)。
图1B为电极与换能器布局图:4×1 高精度 tDCS 电极(中心电极位于 ROI 上方,四个返回电极环绕)与超声换能器(固定于 EEG 电极 C1、C3、FC1、FC3 之间)的相对位置,同时展示 EEG 电极分布。
图1C为超声换能器的自由水扫描结果,显示其聚焦区半高宽(FWHM)为 5 mm(–6 dB),证实 tFUS 的毫米级空间精度。
图1D为刺激时序参数:500 kHz 基频超声以 2 秒为间隔(含随机抖动)施加 200 个试次,脉冲重复频率(PRF)设为 30 Hz(抑制性)或 3 kHz(兴奋性),占空比固定为 30%,串长 500 ms,tDCS 在整个试次中持续接通。
图1为后续所有实验结果的解释提供了技术基础。
HUIYING
tFUS 不能实现源可定位概述
单独 tFUS 在静息态人脑中同时表现出两种属性。一是听觉通路的超阈值效应:3 kHz PRF 诱发 30、90、170 ms 的 ERP(图2A),无论靶向左侧运动皮层还是右侧前额叶,波形与地形图均高度相似(图4B.i),Bayes 因子分析证实二者统计相同(图4B.iii),Granger 因果显示初级听觉皮层→深部脑区的净信息流显著增强(图4C)。二是靶向皮层的亚阈值调节能力:超声压力波打开压电离子通道产生微小去极化(修正 Hodgkin‑Huxley 模型模拟,图6B),虽在 EEG 上无法直接检测,但 itFUS 条件下出现 ROI 与深部脑区间的谱连接解离提示其对靶区网络产生了局部影响。然而,由于听觉通路的超阈值响应淹没了靶区信号,源成像显示同侧 ROI 源活动与对侧无显著差异(图3B),最高活动点与 ROI 距离达 73 mm(etFUS)和 23 mm(itFUS),因此单独 tFUS 无法实现源可定位。

图2 tEAS 诱导半球特异性外源性 ERP 响应
图2从EEG 传感器层面证明 tEAS 可产生半球特异性的外源性响应。
图2A为各条件下预处理的 EEG 蝴蝶图,显示 3 kHz PRF 条件(etFUS、etDCS、etEAS)均出现 30、90、170 ms 三个明显的 ERP 波峰,但仅 tEAS 呈现偏侧化特征。
图2B为置换聚类检验(0–200 ms 窗口,比较同侧 ROI 电极 C1、C3、FC1、FC3 与对侧同源电极)结果:仅 tEAS(etEAS 和 itEAS)出现显著差异聚类(白色圆圈),且两个条件共享 10–63 ms 时间窗口(灰色阴影),而 tFUS 和 tDCS 单独均无显著聚类。
图2C为10–63 ms 窗口平均后的地形图,tEAS 呈现明显的同侧 ROI 聚集(电极 C3 处活动最强),而其他条件呈对称分布。
图2D为电极C3 极性分析(McNemar 检验):itEAS 与 etEAS 在 C3 上产生极性相反的响应,而 tFUS 与 tDCS 单独均无极性效应。
图2首次从传感器层面揭示 tEAS 的特异性效应,并确定后续源成像分析的时间窗口(10–63 ms)。
HUIYING
HD‑tDCS 不能实现源可定位的概述
单独 HD‑tDCS仅具备亚阈值调节能力:阳极或阴极刺激均未在 0-200 ms 窗口产生与刺激时间锁定的 ERP(图2B,无显著聚类),不激活听觉通路,仅通过恒定电场使静息膜电位持续去极化(阳极)或超极化(阴极)(修正 Hodgkin‑Huxley 模型模拟,图6C)。其空间精度虽优于传统 tDCS,但仍局限在厘米级,受容积传导影响显著。源成像显示,单独 tDCS 条件下同侧 ROI 源活动与对侧无显著差异(图3B),最高活动点与 ROI 距离达 73 mm(etDCS)和 26 mm(itDCS),因此自身无法实现源可定位。但它在 tEAS 中扮演关键角色:提供持续的膜电位基线偏移,且其极性决定了 tEAS 响应的符号——在 tEAS 中阳极与阴极条件于电极 C3 上产生极性相反的响应(图2D),而 tFUS 单独无此极性效应)。

图3 tEAS 诱导源可定位的皮层响应
图3从EEG 源成像层面证明 tEAS 可产生与物理靶区空间重合的皮层激活。
图3A为群体平均源图(dSPM,10–63 ms 窗口平均),黑色方框为 ROI(由电极 C1、C3、FC1、FC3 正交投影至皮层定义)。etEAS 与 itEAS 的最高活动区域完全落在 ROI 内,而 tFUS 与 tDCS 单独的最高活动位于听觉皮层或呈弥散分布。
图3B为同侧与对侧 ROI 源活动统计对比(单尾置换 t 检验,FDR 校正):etEAS 同侧(2.59 ± 1.18 zdSPM)显著高于对侧(1.62 ± 0.63 zdSPM);itEAS 同侧(2.40 ± 1.08 zdSPM)显著高于对侧(1.22 ± 0.45 zdSPM);tFUS 与 tDCS 单独均无显著差异。
图3是全文的核心证据,证实 tEAS 是唯一能在静息态人脑中实现源可定位皮层激活的刺激范式。
HUIYING
tEAS(tFUS + HD‑tDCS)实现源可定位的
机理概述
tEAS 实现源可定位的核心机制是非线性协同,将tFUS 的空间特异性亚阈值调节与tDCS 的持续基线偏移叠加,转化为靶区的超阈值输出。修正 Hodgkin‑Huxley 模型(图6A)在传统钠、钾通道外增加压电离子通道,模拟显示:单独超声(压电电流)使膜电位升高但未达阈值(图6B);单独直流电使膜电位偏移但未达阈值(图6C);二者同时施加时,膜电位在超声脉冲时刻超过阈值,产生动作电位(图6D-F)。实验验证包括:传感器层面仅 tEAS 出现同侧与对侧 ROI 电极的显著差异聚类(图2B),10–63 ms 窗口平均后地形图呈现明显的同侧 ROI 聚集(图2C);源成像层面,群体平均源图显示最高活动区域完全落在 ROI(黑色方框)内(图3A),同侧 ROI 源活动显著高于对侧,最高点与 ROI 距离为 0 mm;且该效应无法通过线性叠加 tFUS 与 tDCS 的单独效应复现(图5B),极性由 tDCS 主导且与 tFUS 的 PRF 无关,证明其为非线性协同而非线性相加。
HUIYING
tEAS(tFUS + HD-tDCS)源可定位应用概述
tEAS 作为一种新型非侵入性精准神经调控范式,在基础研究与临床转化中具有独特价值。在基础研究方面,它可在毫秒级时间精度、毫米级空间精度上激活特定皮层区域,用于检验"脑区→行为"的因果关系(优于 TMS 的空间精度和 tDCS 的时间控制),其诱发的时间锁定响应可作为"扰动源"结合 EEG 源成像计算有效连接。在临床转化方面,可精准刺激卒中后病灶周围残存皮层促进神经可塑性,精准靶向抑郁症患者的左侧背外侧前额叶避免传统 tDCS 的电流弥散,以及靶向前扣带回或眶额皮层治疗强迫症/成瘾——这些区域较小且深,tEAS 的毫米级精度具有显著优势。此外,tEAS 可作为脑机接口的稳定"外部激活指令",产生时间锁定、空间精确的皮层信号用于校准或增强控制。其技术优势包括超声物理聚焦(5 mm 半高宽,图1C)带来的空间精度、每个超声脉冲均可稳定引发放电带来的时间锁定性、压电通道+膜电位偏移的透明机制(修正 Hodgkin‑Huxley 模型支持),以及 EEG 源成像可在线验证靶区激活的闭环调控能力。
HUIYING
临床研究
研究方法
受试者:27 名健康志愿者(核心队列),另有扩展队列用于参数优化与可重复性验证(共 11+11+6+8 人)。所有受试者签署知情同意书,实验经 Advarra 机构审查委员会批准。
MRI 与导航:个体 T1‑MRI(3T)用于源成像头模型与超声导航(Localite TMS Navigator)。Sim4Life 仿真计算在体压力(核心队列均值 231 kPa,范围 48.6–372 mW/cm² ISPTA.T),所有参数控制在 FDA 安全指南范围内。
刺激参数:tFUS 为 500 kHz 基频,PRF 30 Hz/3 kHz(扩展至 40、1500、30000 Hz),占空比 30%(扩展至 0.6%、10%、60%,60% 因热感中止),串长 500 ms(压力增强时 100 ms)。HD‑tDCS 为 4×1 环形电极,电流根据个体感知阈值设定(最大 2 mA,均值 1.09 ± 0.52 mA),阳极/阴极,持续接通。tEAS 为二者同时施加。
EEG 记录与处理:64 通道 EEG(BrainCap TMS),1–40 Hz 滤波,独立成分分析去伪迹,共平均参考。源成像采用 dSPM,噪声协方差来自基线窗口(–500 至 –100 ms)。统计分析包括置换聚类检验、置换 t 检验、Bayes 因子、Granger 因果等。
研究结果:
安全性与耐受性:60% 占空比时 4/4 受试者出现头皮热感,实验中止;300 kPa 压力时 2/11 受试者(18.2%)出现头皮热感,中止;其余参数均良好耐受。
单独 tFUS 无法实现源可定位:3 kHz PRF 诱发 30、90、170 ms ERP(图2A),但靶向不同脑区时波形相同(图4B.i),Bayes 因子证实统计相似(图4B.iii)。Granger 因果显示 A1→深部脑区信息流显著增强,而 ROI→深部脑区无变化(图4C)。源成像显示同侧与对侧 ROI 源活动无差异(图3B),最高点距 ROI 73 mm(etFUS)和 23 mm(itFUS)。参数扩展(PRF 40、1500 Hz,占空比 0.6%、10%)及压力增强(300 kPa)均未改善。

图4 tFUS 诱导的听觉通路超阈值响应
图4证明单独 tFUS 的 ERP 源于听觉通路,与靶区位置无关。
图4A为3 kHz PRF tFUS(etFUS)在 20-40、80-100、160-180 ms 三个 ERP 峰值的 EEG 地形图与源成像图:地形图呈对称分布,源成像显示活动位于听觉皮层或深部脑区,而非靶区 ROI。
图4B为靶区对比实验:将 tFUS 分别作用于左侧运动皮层(LH M1)与右侧前额叶(RH PFC),图4Bi显示二者波形与地形图高度相似;图4Bii为置换聚类检验,无显著差异聚类;图4Biii为Bayes 因子分析(log₁₀ BF < 0 支持零假设),在 10-63、20-40、80-100 ms 窗口所有电极均提供稳健证据支持两种条件响应相同,160-180 ms 窗口对中‑大效应量仍支持相同。
图4C为Granger 因果分析:etFUS 与 itFUS 均显著增强初级听觉皮层(A1)→深部脑区的净信息流,而 ROI→深部脑区无显著变化。
图4阐明单独 tFUS 的“超阈值效应”本质上是听觉通路激活,而非靶区皮层刺激。
单独 HD‑tDCS 无法实现源可定位:无时间锁定 ERP(图2B),源成像显示同侧与对侧 ROI 源活动无差异(图3B),最高点距 ROI 73 mm(etDCS)和 26 mm(itDCS)。
tEAS 稳定实现源可定位:置换聚类检验显示仅 tEAS 出现同侧与对侧 ROI 电极显著差异(图2B),10–63 ms 窗口地形图呈现同侧 ROI 聚集(图2C)。源成像显示最高活动区域完全落在 ROI 内(图3A),同侧 ROI 源活动显著高于对侧,最高点与 ROI 距离为 0 mm。极性由 tDCS 主导(图2D),与 PRF 无关。该效应非叠加(图5B),7天洗脱后仍可重复。

图5 tEAS 效应非叠加,非 tDCS 剂量线性相关
图5通过三项分析证明tEAS 的非线性协同机制。
图5A‑B将tFUS 与 tDCS 单独条件下的源活动线性相加,无法复现 tEAS 的同侧增强效应(p > 0.05)。
图5C‑E回归分析显示 tEAS 的 ROI 响应与 tFUS 强度、tDCS 头皮电流、tDCS 皮层电流均无显著线性相关(R² < 0.05,p > 0.05)。
图5排除“tEAS 仅为两种刺激线性叠加”或“效应由剂量简单决定”的可能性,支持非线性协同机制。
机制模型验证:修正 Hodgkin‑Huxley 模型显示,单独超声或单独直流电均不引发动作电位,二者同时施加时超过阈值产生放电(图6D–F)。

图6 修正 Hodgkin‑Huxley 模型模拟压电‑直流协同
图6通过修正Hodgkin‑Huxley模型,为tEAS的非线性协同机制提供了生物物理层面的验证。
图6A在传统钠、钾、漏通道基础上并联增加一个压电离子通道,其开放概率随超声压力变化,模拟tFUS的机械敏感性。
图6B显示单独施加模拟tDCS的亚阈值直流电(阳极或阴极),膜电位发生持续偏移但未达动作电位阈值;
图6C显示单独施加模拟tFUS的压电电流(超声脉冲),膜电位发生短暂去极化同样未达阈值。
图6D将阳极直流电(去极化偏移)与超声压电电流同时施加,膜电位在超声脉冲期间超过阈值产生动作电位,模拟etEAS的协同效应;
图6E将阴极直流电(超极化偏移)与超声压电电流同时施加,膜电位上升但仍低于阈值,对应itEAS在单次模拟中可能低于阈值的情况(实验中发现itEAS仍有响应但极性相反)。
图6F放大显示图6D的动作电位波形,清晰展示快速去极化与复极化过程。该模型证明:单独tFUS或tDCS均仅为亚阈值调节,二者协同时可通过非线性叠加转化为超阈值输出,且极性由tDCS主导,与实验结果高度一致。
HUIYING
总结
本研究系统阐明了 tFUS 与 HD‑tDCS 在静息态人脑中的作用机制,并首次证明二者协同(tEAS)可实现源可定位的皮层激活。单独 tFUS 具有听觉通路的超阈值效应(30、90、170 ms ERP,A1→深部脑区 Granger 因果显著)和靶向皮层的亚阈值调节能力(压电通道开放),但因听觉响应淹没靶区信号而无法实现源可定位(同侧 vs. 对侧 ROI 源活动无差异,最高点距 ROI 73/23 mm)。单独 HD‑tDCS 仅提供持续的膜电位基线偏移(亚阈值调节),空间精度有限(厘米级),同样无法实现源可定位(同侧 vs. 对侧无差异,最高点距 ROI 73/26 mm)。tEAS 通过非线性协同机制——tFUS 的脉冲式压电电流(空间特异性,毫米级)与 tDCS 的持续基线偏移叠加——将亚阈值调节转化为超阈值输出,在传感器层面(仅 tEAS 出现同侧 vs. 对侧显著差异聚类,图2B)、地形图(同侧 ROI 聚集,图2C)和源成像层面(最高活动点与 ROI 重合,图3A;同侧源活动显著高于对侧,Cohen’s d > 1.0,图3B)均获得一致验证,且该效应非叠加、极性由 tDCS 主导、与 PRF 无关、可重复性良好。修正Hodgkin‑Huxley 模型(图6)为这一协同机制提供了生物物理基础。该研究为精准非侵入性神经调控提供了机制透明、空间物理聚焦(5mm半高宽,图1C)、时间精确可控(毫秒级锁定)的新范式,在认知神经科学、神经康复和精神疾病干预领域具有重要的基础与转化价值。
-
传感器
+关注
关注
2577文章
55445浏览量
793739 -
医疗电子
+关注
关注
31文章
1459浏览量
92223 -
脑机接口
+关注
关注
10文章
438浏览量
22555
发布评论请先 登录
多任务TDCS车站分机通信协议的设计
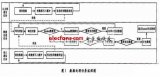
基于铁路专用线改造的TDCS系统设计与应用
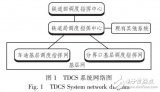
基于存储转发机制的远距航空通信TDCS模型

UWB达到毫米级定位精度!恩智浦携手合作伙伴实现新突破
如何科学评估HD-tES对上肢功能的改善(fNIRS)

泡沫起升仪步进/伺服电机细分驱动技术:实现冲程毫米级定位的电子方案

闭眼是tDCS经颅电刺激的最佳状态?

tFUS技术标准化指南:参数、设备、实验与安全全流程

tFUS如何精准调参实现神经活动的双向调节?

聚焦tFUS与非聚焦tUS其神经调控机理若何?

tFUS如何有效的脑肿瘤干预?

tFUS工程化的关键在哪里?

可穿戴的tFUS工程化关键路在何方?




 tFUS+HD-tDCS如何实现毫米级皮层精准调控?
tFUS+HD-tDCS如何实现毫米级皮层精准调控?




评论