单脉冲 TMS是指每次只释放一个磁刺激脉冲,用于评估大脑皮层在某一时刻的兴奋性状态。当单脉冲TMS作用于初级运动皮层(M1) 时,会激活皮质脊髓束,在对应的靶肌肉上记录到一个电生理信号,即运动诱发电位(MEP)。如图1a所示,TMS作用于M1后,产生下行冲动,经脊髓运动神经元,最终在目标肌肉(如第一骨间背侧肌)表面通过肌电图(EMG)记录到MEP。MEP是评估皮质脊髓束完整性和皮层兴奋性的核心指标,其波形特征可反映从皮层到肌肉整个通路的整合功能。
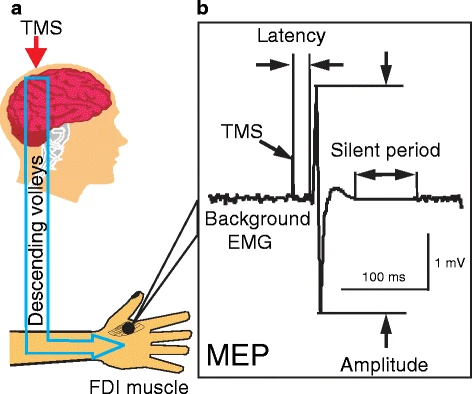
图1:TMS作用原理与MEP测量方法
图1a和图1b两部分组成。图1a展示了TMS作用于初级运动皮层(M1)后,下行冲动经皮质脊髓束、脊髓运动神经元,最终在目标肌肉(如第一骨间背侧肌)记录到运动诱发电位(MEP)的完整通路。图1b则标注了MEP的关键测量参数:潜伏期Latency(从刺激到MEP起始的时间)、振幅Amplitude(波峰到波谷的电压差值)以及静默期Selent period(从MEP结束或起始至背景肌电恢复的时间)。图1直观地定义了单脉冲TMS的核心评估指标,为后续理解各疾病中MEP异常奠定了基础。
HUIYING
单脉冲 TMS 如何评估 MEP
单脉冲TMS通过调节刺激强度和被试肌肉状态,可测量以下参数(见图1b):
运动阈值MEP:分为静息运动阈值(肌肉放松时能引发微小MEP的最小刺激强度)和活动运动阈值(肌肉轻度收缩时的最小刺激强度)。阈值高低反映皮层中最敏感神经元群的兴奋性。
MEP 振幅Amplitude:通常测量波峰-波谷的电压差值。振幅越大,说明皮质脊髓通路整体兴奋性越高。
MEP 潜伏期Latency:从刺激发出到MEP起始点的时间间隔,反映神经传导速度。
静默期Silent period:在自主收缩肌肉时给予TMS,MEP之后会出现一段EMG中断(无电活动)。静默期的后段主要由皮层内GABA_B受体介导的抑制效应决定。如图1b标注,MEP潜伏期从刺激开始到MEP onset,振幅为峰-峰值,静默期可从MEP结束或 onset 开始测量至背景EMG恢复。
这些参数在不同神经退行性疾病中呈现特征性改变,例如PD患者MEP振幅增高、静默期缩短;ALS患者早期阈值降低、晚期升高。
HUIYING
成对脉冲 TMS 定义
成对脉冲 TMS是指在同一皮层区域先后施加两个磁刺激脉冲:条件刺激(S1) 和 测试刺激(S2)。通过改变两脉冲之间的刺激间隔(ISI) 和刺激强度,可以探测皮层内不同抑制性或易化性神经回路的功能状态。S1 对 S2 诱发的 MEP 产生抑制或易化作用,反映特定回路的兴奋性。
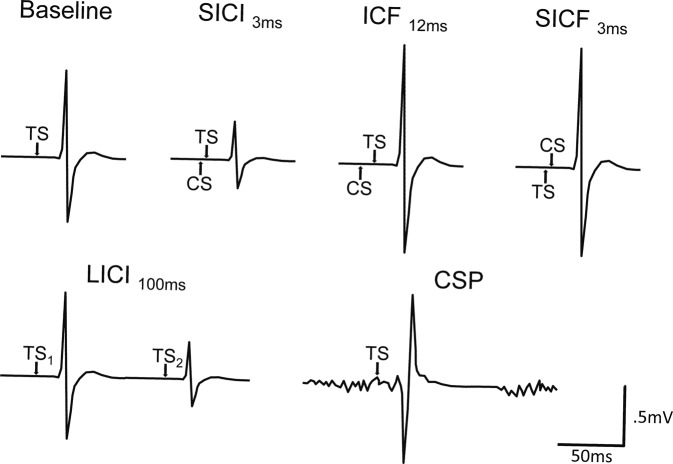
图2:典型TMS刺激协议下的肌电反应示意图
图2展示了五种经颅磁刺激(TMS)协议下典型的肌电反应波形,包括:短间隔皮层内抑制(SICI,3 ms脉冲间隔) 表现为测试刺激诱发的运动诱发电位(MEP)幅值显著低于基线单脉冲MEP,反映GABA_A介导的快速抑制;皮层内易化(ICF,12 ms间隔) 表现为MEP幅值高于基线,反映谷氨酸能(尤其NMDA受体)介导的兴奋性增强;短间隔皮层内易化(SICF,3 ms间隔但刺激强度不同) 用于排除SICI测量中I‑波易化成分的干扰;长间隔皮层内抑制(LICI,100 ms间隔) 表现为第二个MEP幅值明显小于第一个MEP,反映GABA_B介导的慢速抑制;以及皮层静默期(CSP) 在持续肌肉收缩时单脉冲TMS后出现的一段EMG电活动完全消失的间歇,其长度整合了GABA_A与GABA_B的抑制作用。
HUIYING
成对脉冲 TMS 评估的皮层回路
短间隔皮层内抑制(SICI)与皮层内易化(ICF)
核心概念描述:SICI 评估“刹车”系统(GABA能抑制)是否失灵,ICF 评估“油门”系统(谷氨酸能兴奋)是否过度或不足。两者共同反映 皮层内兴奋-抑制平衡,这种平衡是正常运动控制、认知功能、甚至情绪调节的基础。阈下条件刺激(S1)是强度低于运动阈值、本身不引发MEP的“调节”脉冲;阈上测试刺激(S2)是强度高于运动阈值、能稳定引发MEP的“测试”脉冲。两者通过同一线圈、以极短时间间隔(1~5 ms)先后施加于同一皮层区域,通过观察S2的MEP是否被S1抑制,来量化皮层内GABA_A介导的快速抑制(SICI)。
在成对脉冲TMS中,当ISI从1 ms逐渐增加到30 ms时,MEP幅度通常表现为:
早期抑制(约1~5 ms):SICI,由GABA_A介导。
早期易化(约6~8 ms):第一个易化峰(peak 1),可能与谷氨酸能兴奋性回路的快速激活有关。
中期抑制(约9~12 ms):第一个抑制谷(trough 1),可能是抑制与易化相互作用的结果。
中期易化(约13~20 ms):第二个易化峰(peak 2)。
晚期抑制(约20~25 ms):第二个抑制谷(trough 2)。
晚期易化(约25~30 ms):第三个易化峰(peak 3)。这些波动的产生是由于皮层内不同时间常数的兴奋性和抑制性中间神经元先后激活,它们的总和效应在时间上形成交替的波形。
| 峰/谷 | 时间范围 | 主导回路 | 神经递质/受体 | 病理改变(PD) |
| peak 1 | 6-8 ms | 局部兴奋性回路 | 谷氨酸(AMPA受体) | 异常增高 |
| trough 1 | 9-12 ms | 早期抑制反馈 | GABA_A / GABA_B(突触前) | 消失(转为易化) |
| peak 2 | 13-18 ms | 循环兴奋 | 谷氨酸(NMDA参与) | 异常增高 |
| trough 2 | 19-23 ms | 晚期抑制 | GABA_B(突触后) | 消失(转为易化) |
| peak 3 | 25-30 ms | 皮层-皮层易化 | 谷氨酸 + 神经调节 | 异常增高 |
方法:S1 为阈下强度,S2 为阈上强度,ISI 1~5 ms 时 MEP 被抑制(SICI),ISI 7~30 ms 时 MEP 被易化(ICF)。
机制:SICI 主要由 GABA_A 受体介导;ICF 可能与谷氨酸能环路有关。
临床意义:在PD 中 SICI 减弱、ICF 增强,提示皮层去抑制。如图3所示,PD患者在停药状态下,SICI 在多个ISI点(如1 ms、易化峰1、谷1等)显著降低(MEP%从约50%升至130%甚至更高),用药后部分恢复。图中对比了健康对照、PD OFF(停药)、PD ON(服药)三组,直观展示了抑制-易化失衡。
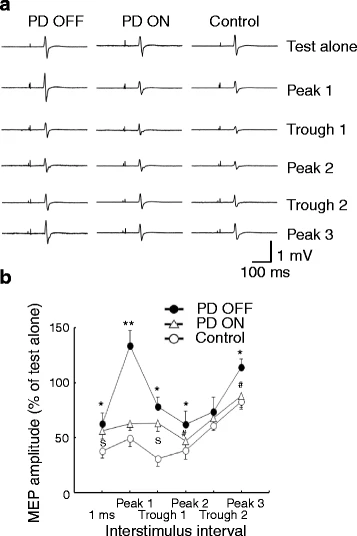
图3:帕金森病患者短间隔皮层内抑制(SICI)的异常表现
图3分为a(示例波形)和b(组数据统计)。图3a显示了一名健康对照、一名PD患者服药前(OFF)和服药后(ON)在不同刺激间隔下的MEP波形,可见PD OFF状态下SICI明显减弱(抑制波形消失甚至转为易化)。图3b以百分比形式汇总了多组数据:PD OFF组在多个刺激间隔(如1 ms、易化峰1、谷1、峰2、峰3)的SICI显著低于健康对照,表现为抑制程度下降(MEP%从约50%升至130%以上);PD ON组部分间隔得到改善,但1 ms和谷1处仍未完全恢复正常。图3有力地说明了PD患者皮层内GABA_A介导的抑制功能受损,且多巴胺能药物可部分逆转这一缺陷。
长间隔皮层内抑制(LICI)
核心概念说明:长间隔皮层内抑制(LICI)是一种通过双脉冲经颅磁刺激(两个阈上刺激,间隔50–200毫秒)评估大脑皮层抑制功能的电生理指标,其核心机制是GABA_B受体介导的持续性突触后抑制:第一个刺激不仅诱发运动诱发电位(MEP1),还激活局部GABA能中间神经元释放GABA,作用于突触后GABA_B受体,产生长达100毫秒以上的超极化效应,从而抑制皮层兴奋性,使第二个刺激诱发的MEP2幅度显著降低。LICI主要反映大脑“慢刹车”系统的功能完整性,在帕金森病、抑郁症等疾病中常表现为抑制减弱,并可作为预测疾病进展或监测治疗反应的客观生物标志物。(如图2)
方法:S1 和 S2 均为阈上强度,ISI 50~200 ms。
机制:主要由 GABA_B 受体介导。
临床意义:PD 患者 LICI 降低,与静默期缩短一致。
传入抑制(SAI 和 LAI)
方法:先给予外周神经电刺激(如正中神经),再给予 M1 TMS,ISI 约20 ms(SAI)或200 ms(LAI)。
机制:感觉传入对 M1 的抑制作用,SAI 反映胆碱能通路功能。
临床意义:AD、PD、HD 中 SAI 均下降,提示胆碱能缺损。图4展示了 PD 患者在用药状态下 SAI 减弱(MEP 比值接近1,无抑制),而联合丘脑底核深部脑刺激(STN DBS)后可恢复抑制(MEP 比值降至0.6左右),表明DBS 可改善感觉运动整合。图4是通过比较PD患者在药物ON/OFF和DBS ON/OFF四种状态下SAI的变化推导出来的:药物单独使用使SAI从正常(抑制)变为异常(无抑制),而联合STN-DBS后SAI恢复至正常,从而证明DBS可以纠正药物诱发的传入抑制障碍。
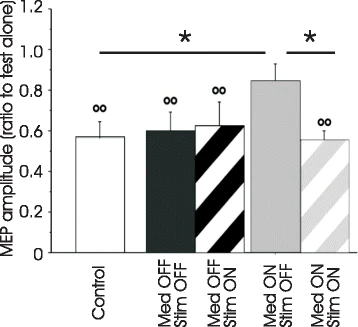
图4:丘脑底核深部脑刺激对帕金森病患者传入抑制(SAI)的调节作用
图4以柱状图比较了健康对照和PD患者在四种状态(药物OFF/ON、刺激OFF/ON)下的短潜伏期传入抑制(SAI)程度,纵坐标为MEP比值(小于1表示抑制)。结果显示:健康对照的SAI明显(比值约0.5);PD患者药物OFF时SAI正常(与对照无差异);但药物ON时SAI显著减弱(比值接近1,无抑制);而药物ON联合STN-DBS(刺激ON)时,SAI恢复到健康对照水平(比值再次降至约0.5)。图4揭示了多巴胺与感觉运动整合之间的复杂交互,并证明STN-DBS可以纠正药物诱发的传入抑制障碍,改善本体感觉处理。
半球间抑制(IHI)
方法:双侧 M1 各放一个线圈,条件刺激一侧 M1,测试刺激对侧 M1,ISI 约10 ms(短 IHI)或50 ms(长 IHI)。在IHI范式中,条件刺激是首先施加于一侧M1的阈上刺激,用于启动跨胼胝体抑制;测试刺激是随后施加于对侧M1的阈上刺激,用于检测抑制效果。两者都是阈上强度,但分别作用于两个半球。
机制:通过胼胝体介导。
临床意义:伴有镜像运动的 PD 患者长 IHI 减弱。
小脑抑制(CBI)
方法:小脑刺激后5~7 ms 给予 M1 刺激,观察 MEP 抑制。
机制:小脑-丘脑-皮层通路。
临床意义:PD 患者 CBI 减弱,与姿势性震颤相关。
HUIYING
重复 TMS(rTMS)与 LTP/LTD 样可塑性
重复 TMS 是指以固定频率连续施加多个 TMS 脉冲。不同频率产生相反的效应:
高频 rTMS(≥5 Hz):易化皮层兴奋性,可诱导长时程增强(LTP)样可塑性,效应可持续数分钟至数小时。
低频 rTMS(≤1 Hz):抑制皮层兴奋性,可诱导长时程抑制(LTD)样可塑性。
这种可塑性变化被认为是突触功效的持久改变,是 rTMS 发挥治疗作用的基础。多次重复应用(多疗程)可使效应延长至数周或数月。
HUIYING
可塑性诱导范式:PAS 与 TBS
配对关联刺激(PAS)
方法:反复将外周神经电刺激与M1 TMS 配对,两者间隔约25 ms,使感觉输入和皮层刺激几乎同时到达 M1。
效应:可诱导 LTP 样 MEP 易化,反映 Hebbian 可塑性。
临床发现:PD 患者停药时 PAS 诱导的可塑性受损,药物或 DBS 可恢复(见图5)。PAS是一种通过精确时间配对(感觉输入+TMS)诱导皮层LTP样可塑性的范式。PD患者这种可塑性受损,图5证明:只有左旋多巴与STN-DBS联合使用才能使其完全恢复正常,单一治疗仅能部分改善。这揭示了药物与DBS协同恢复突触可塑性的关键机制。
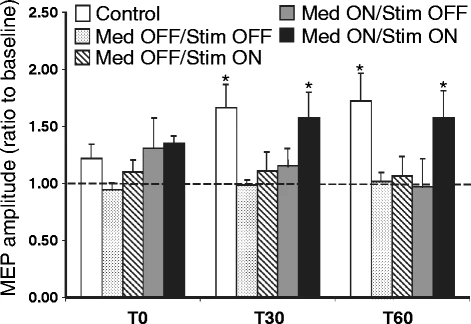
图5:丘脑底核深部脑刺激与药物协同恢复帕金森病患者皮层LTP样可塑性
图5展示了PAS干预后0、30、60分钟时MEP振幅相对于基线的变化(比值>1表示易化)。健康对照组在PAS后MEP升至约150%,表现出典型的LTP样可塑性。PD患者在“药物OFF+刺激OFF”状态下MEP始终在100%附近,无可塑性。单独“药物ON”或单独“刺激ON”状态下,MEP虽有轻微升高但未达正常水平。仅在“药物ON+刺激ON”联合状态下,MEP在30和60分钟后均升高至约150%,与健康对照组相当。图5强有力地证明:皮层可塑性的恢复需要多巴胺能药物与深部脑刺激的协同作用,这为理解DBS的治疗机制和优化PD康复策略提供了关键神经生理学证据。
θ爆发刺激(TBS)
方法
TBS是以高频(50 Hz) 脉冲组成一个“爆发”(burst),每个爆发内包含3个脉冲,每200毫秒重复一次该爆发(即5 Hz的重复频率)。
两种模式:
间歇性TBS(iTBS):刺激2秒,间歇8秒,重复多次(总刺激时间约3分钟)。易化皮层,诱导LTP样可塑性(MEP幅度增加)。
持续性TBS(cTBS):连续刺激40秒(无间歇)。抑制皮层,诱导LTD样可塑性(MEP幅度降低)。
优势
刺激时间极短:iTBS约3分钟,cTBS约40秒,远低于传统rTMS(10-30分钟)。
效应强且持久:单次TBS可产生持续30-60分钟的皮层兴奋性改变,且重复应用效果可累积。
受试者耐受性好:因刺激时间短,不适感轻微。
HUIYING
临床研究
本文对四种神经退行性疾病进行了系统综述,主要研究方法为:
横断面或纵向队列研究,比较患者与健康对照的 TMS 参数;
干预研究:使用 rTMS 或可塑性范式,评估症状改善或皮层兴奋性变化。
主要研究结果
| 疾病 | 单/成对脉冲 TMS 异常 | 可塑性异常 | rTMS 治疗效果 |
| PD | MEP 振幅↑,静默期↓,SICI↓,ICF↑,SAI 药物后↓ | PAS 诱导的 LTP 样可塑性受损,药物或 DBS 可部分恢复 | 高频 rTMS(M1)改善运动症状;低频 rTMS(SMA)减轻异动症 |
| AD | SAI↓(早期即可出现),SICI 不一致,ICF 正常 | LTP 样可塑性受损,LTD 样可塑性相对保留 | 高频 rTMS(双侧 DLPFC)改善记忆和语言功能 |
| ALS | MEP 阈值早期↓晚期↑,MEP 振幅↑,静默期↓,SICI 显著↓ | 未明确 | 高频 rTMS 效果有限甚至有害;低频 rTMS/cTBS 有初步但不确定的益处 |
| HD | MEP 阈值↑,振幅↓,静默期进行性缩短,SAI↓ | LTP 和 LTD 样可塑性均受损 | 低频 rTMS(SMA)减轻舞蹈样动作 |
HUIYING
总结
经颅磁刺激(TMS)是一种无创、安全且信息丰富的人脑刺激技术。通过单脉冲、成对脉冲、重复脉冲及可塑性诱导范式,可以分别评估:
皮层脊髓束的兴奋性(MEP 阈值、振幅、潜伏期、静默期);
皮层内抑制/易化回路(SICI、LICI、ICF);
感觉-运动整合(SAI、LAI);
半球间和小脑-皮层通路(IHI、CBI);
突触可塑性(PAS、TBS)。
在帕金森病、阿尔茨海默病、肌萎缩侧索硬化和亨廷顿病中,TMS揭示了特征性的皮层兴奋性改变和可塑性缺陷,这些异常与疾病的病理生理机制(GABA能、胆碱能、谷氨酸能障碍)高度吻合。同时,rTMS 作为一种治疗手段,已在部分疾病中显示出症状改善潜力,尤其是高频 rTMS 对 PD 运动症状和 AD 认知功能的益处。然而,TMS 临床转化仍面临挑战:测量变异大、缺乏早期生物标志物、治疗效果偏弱且短暂。未来需要更大规模的假刺激对照研究,并探索 TMS 与药物、深部脑刺激、神经影像等技术的联合应用,以推动其成为常规诊疗工具。
-
医疗电子
+关注
关注
31文章
1461浏览量
92223 -
电刺激装置
+关注
关注
0文章
50浏览量
5792
发布评论请先 登录
看过那么多文章,你真的了解ZigBee吗?
看了那么多c语言书籍,还是这本好!
人为什么会有那么多烦恼?
为什么加入反馈后,运放增益变小那么多?
经颅电刺激系列之高强度经颅交流电刺激Hi-tACS

经颅电刺激系列之高精度经颅电刺激HD-TES

经颅电刺激系列之时域相干电刺激tTIS

时间干涉经颅磁刺激TI-TMS是经颅磁的未来吗




 经颅磁那么多模式都管啥?
经颅磁那么多模式都管啥?





评论