X 疾病是世界卫生组织 (WHO) 于 2018 年创造的术语,指一种新出现的病原体或具有新获得大流行潜力的先前已知病原体(Simpson等人,2020)。根据这一定义,由严重急性呼吸综合征冠状病毒 2 (SARS-CoV-2) 引起的 COVID-19 是第一种 X 疾病,但将来可能还会出现另一种疾病。对抗新型病毒的威胁,最有力、最有效的武器是阻止其传播,其要点是准确的早期诊断和有效的隔离。家庭检测通常通过智能手机应用程序向公共卫生当局报告结果,是该策略中的一个关键工具,使个人能够在不前往医疗机构的情况下立即识别感染,从而降低传播风险并保存个人防护设备。然而,目前的家庭检测,无论是基于抗原检测还是等温扩增,都表现出灵敏度的局限性,特别是在无症状个体中,并且要求用户适当地自行采集鼻拭子样本。获得优质样本仍然是一个重大挑战,因为劣质样本通常会导致结果不可靠。尽管制造商提供视觉教具和教学视频来指导用户,但自我收集的能力随着年龄的不同而存在很大差异,特别是对于需要成人帮助以避免因操作不当而损坏鼻腔的幼儿。这些挑战凸显了迫切需要更强大和用户友好的家庭检测平台,以最大限度地减少操作员依赖并提高检测准确性,特别是在无症状感染时期。因此,理想的呼吸道病毒家庭检测平台应整合以下关键特性:(i)非侵入性且用户友好的样本采集,(ii)能够检测症状前感染的高灵敏度,(iii)快速检测时间(<10分钟),(iv)操作简单,无需外源试剂或复杂的处理步骤,以及(v)无缝结果报告的连接性。
本文推出了 EBCatch,这是一种直接从呼出气体冷凝物 (EBC) 中对呼吸道病毒进行无标记电化学检测的集成系统。该平台结合了基于半导体的冷凝器,可在 1 分钟内高效收集 EBC,这是一种基于碳纳米管的电化学生物传感器,具有 ACE2 功能无需外源试剂或复杂的样品预处理,EBCatch 即可实现飞克级灵敏度(假病毒的检测限为 1.6 fg/mL,远低于 SARS-CoV-2 感染者的 EBC 样本中的病毒载量),并可在 8 分钟内从样本采集到读出结果,从而证明诊断准确性很高,灵敏度高达 95.06%。特异性为 97.30%,总体准确度为 96.13%,能够在症状前和抗原阴性阶段进行检测。值得注意的是,EBCatch 反应不仅反映了病毒载量,还反映了病毒活动,为了解感染状态和传播风险提供了宝贵的见解。这种多功能且用户友好的平台代表了家庭呼吸道感染分散式实时监测的重大进步,从而能够在新出现的疫情爆发期间进行及时干预。
EBCatch 的操作流程如图 1a 所示,并通过三个关键步骤进行:(1)EBC 收集,该过程从用户向连接到半导体制冷模块的一次性、符合人体工程学的吸嘴轻轻呼气开始。该系统可有效冷凝呼吸气溶胶,通常可在 30 秒内产生足够量的 EBC(约 80 μL)用于分析,最大限度地减少用户不适以及样品稀释或降解的风险,从而克服传统基于面罩或商业冷凝器方法的主要局限性。 (2) 无标记电化学检测,将少量 EBC 直接滴入一次性 ACE2 功能化 SPE 中,并通过 i-t 实时测量,无需试剂,可在 30 秒内快速读出 (3) 通过专用智能手机应用程序进行自动分析,使用预定义阈值对 i-t 结果进行分类,并在 30 秒内提供诊断结果(阳性/阴性/重新测试)。这种从样本采集到结果交付的集成工作流程可在 8 分钟内完成,使 EBCatch 成为早期感染筛查(包括无症状窗口期)的实用解决方案。

集成 EBCatch 平台的示意图及其用于家庭 EBC 收集和分析的关键性能指标。 (a) 家庭测试集成 EBCatch 程序示意图,从样本采集到结果输出可在 8 分钟内完成。 (b) EBC 收集器的分解图,详细说明了其关键部件,包括 (i) 制冷模块、(ii) 气流通道和 (iii) 一次性装置。 (c) 通过连续温和呼气收集的 EBC (VEBC) 体积。数据表示为平均值±SD(n = 23 个独立样本)。 (d) 从 20 名阴性志愿者 1 分钟呼气期间收集的 VEBC。数据以平均值±标准差表示(n = 每个志愿者 5 次重复)。 (e) 3 分钟内从 20 名阴性志愿者和 16 名阳性志愿者收集的 VEBC 的比较,n = 120(左)和 96(右)。 (f) 按照 EBC 收集程序,针对五个标准的用户满意度调查评级(等级 1-5)。 (g) 不同采样深度和技术的鼻拭子抗原测试的代表性结果。 (h) 对来自 COVID-19 阳性和康复志愿者的匹配 EBC 和鼻拭子样本进行 qRT-PCR 分析。从确诊的 COVID-19 个体在整个感染期间收集的连续 EBC 样本的 (i) qRT-PCR Ct 值和 (j) i-t 响应的动态。数据表示为平均值±SD (n = 3)。

Fig. 2. Fabrication process and analytical characterization of the ACE2/PBA/SWCNT/SPE sensor via ferricyanide-dependent system. (a) Schematic illustration of the stepwise modification process for fabricating the ACE2/PBA/SWCNT/SPE sensor. (b) CV responses of the electrode in a 5 mM K3[Fe(CN)6]/K4[Fe(CN)6] solution after each modification step. (c) CV curves at various scan rates (0.005–0.2 V/s) and (d) the linear fitting of the peak currents (Ipa and Ipc) versus v1/2 for ACE2/PBA/ SWCNT/SPE. (e) DPV responses and (f) the corresponding calibration curves of the ACE2/PBA/SWCNT/SPE sensor to various concentrations of SP. (g) Long-term stability of the ACE2/PBA/SWCNT/SPE and ACE2/SWCNT/SPE sensors after storage at 4 ◦C. Data are presented as mean ± SD (n = 3).

Fig. 4. Fabrication process and analytical characterization of the ACE2/PBA/SWCNT/SPE sensor in PBS for virus detection. (a) CV responses in PBS of the sensors including bare SPE, SWCNT/SPE, PBA/SWCNT/SPE, ACE2/PBA/SWCNT/SPE without or with BSA blocking, ACE2/PBA/SWCNT/SPE (with BSA) in the presence of SP (SP1: 1 μg/mL; SP2: 10 μg/mL). (b) The i-t response curves of the sensor with and without ACE2 functionalization towards SP and PSV. The i-t response curves of the sensor with and without PBASE modification towards (c) SP and (d) PSV. Calibration curves of the ACE2/PBA/SWCNT/SPE sensor for (e) SP and (f) PSV detection. Data are presented as mean ± SD (n = 3). (g) The i-t response curve of the sensor towards SARS-CoV-2, SARS-CoV, and their mixture. (h) Specificity analysis of the sensor towards SARS-CoV-2 and other respiratory viruses (SARS-CoV-2: 1 μg/mL; interferents: 10 μg/mL). (i) Specific responses of sensors functionalized with different receptors (ACE2, ACE, CD26) towards their corresponding target viruses. Data are presented as mean ± SD (n = 3).

Fig. 5. Smartphone-based automated analysis and clinical performance of the EBCatch platform. (a) Software interface of the smartphone app for automated data processing and diagnostic readout. Representative i-t curves and the corresponding classification results for (b) negative, (c) positive, and (d) questionable samples requiring retest. (e) Pie chart showing the proportion of negative and positive participants among the total volunteers. (f) Distribution of infection symptoms among the 16 positive volunteers. (g) Information on the SARS-CoV-2 strain types and the corresponding number of infected individuals. The (I-I0)/I0 response for EBC samples from (h) 20 negative cases and (i) 16 positive cases. Data are presented as mean ± SD (n = 3). (j) Box plot of the (I-I0)/I0 response for negative and positive EBC samples with the diagnostic threshold, n = 60 (left) and 48 (right).
文献链接
https://doi.org/10.1016/j.bios.2026.118721
来源:生物传感器
-
电化学传感器
+关注
关注
3文章
82浏览量
15795 -
生物传感器
+关注
关注
12文章
405浏览量
38648
发布评论请先 登录
MAX30131/MAX30132/MAX30134:电化学传感器AFE的卓越之选
中国海洋大学:在食品生物传感器开发研究领域取得新进展!

中科院长春应化所张强团队:面向持续无创健康监测的可穿戴汗液电化学生物传感器

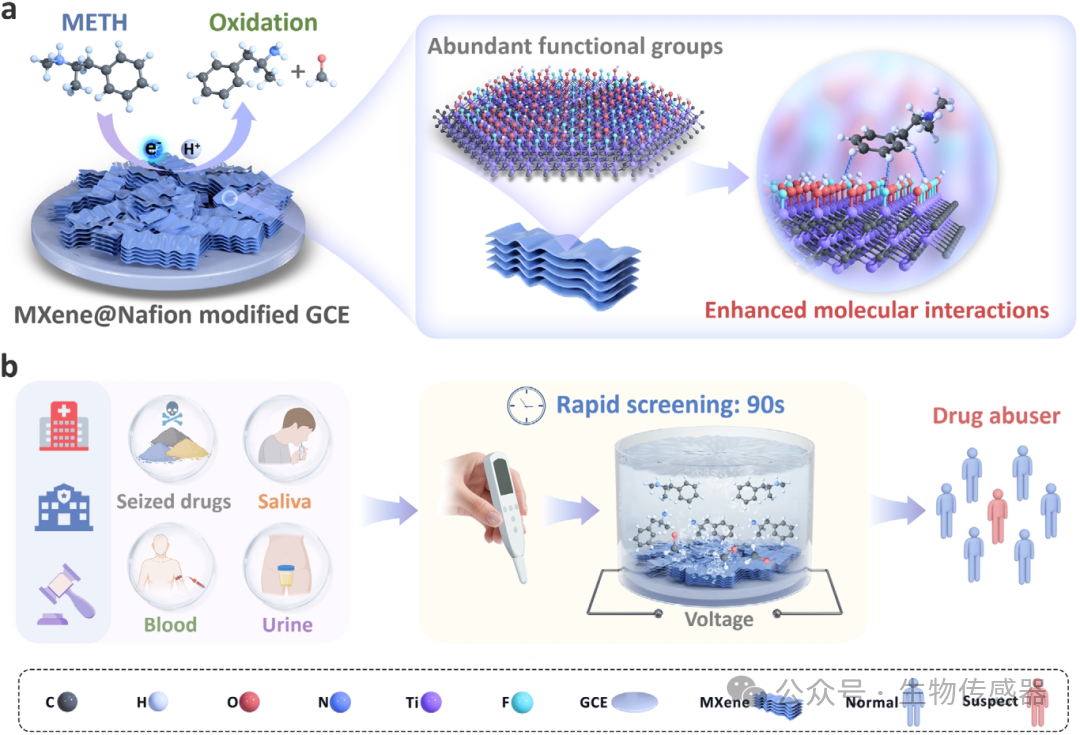
中国科学院深圳先进院:研制一种MXene 电化学传感器秒级精准检测冰毒
探索SGX_EVAL_EC电化学气体传感器评估套件:开启气体传感器设计新征程
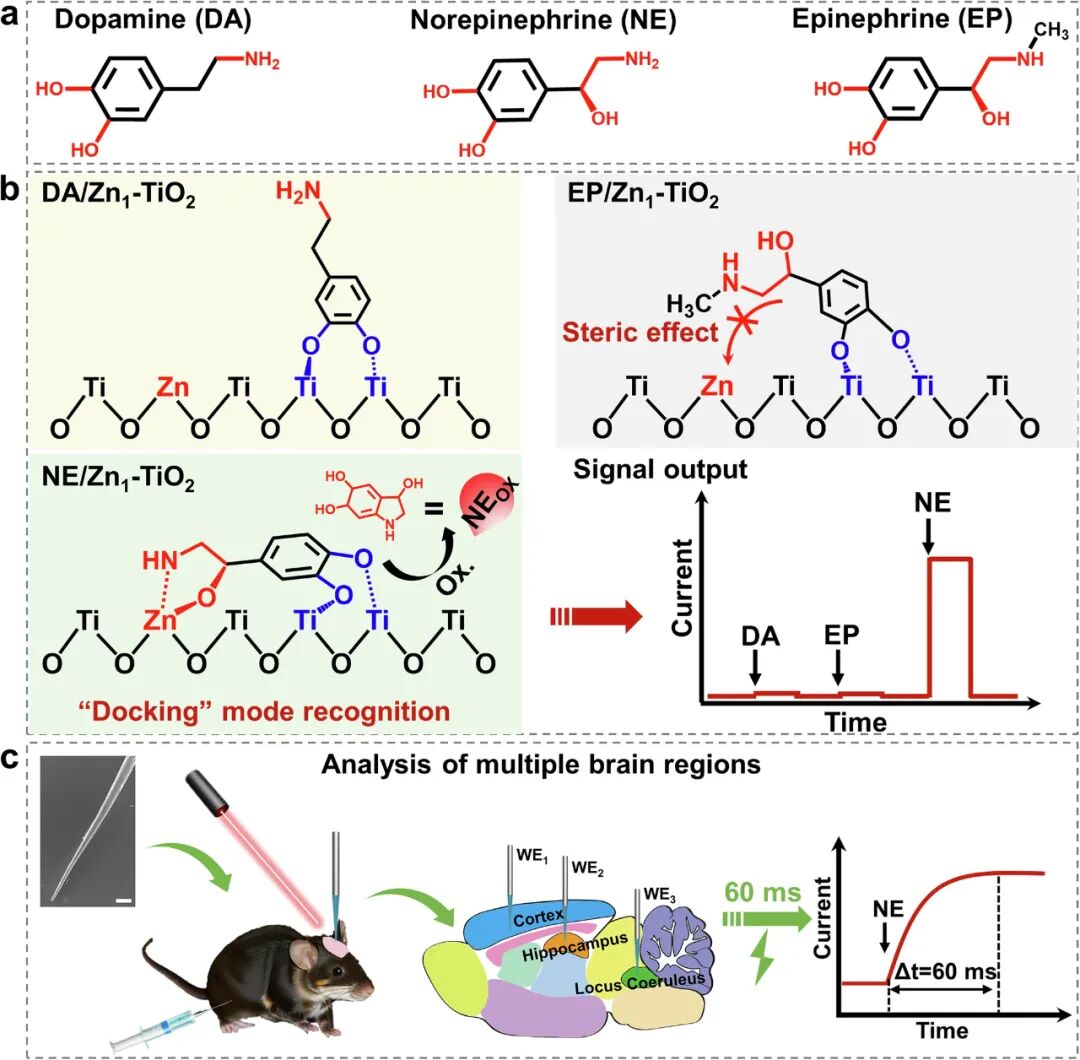
华东师范大学:用于去甲肾上腺素传感和癫痫脑区协同作用的单原子光电化学生物传感器
求助,怎么提高电化学式CO传感器的精度?
北京理工大学生命学院:研发新型电化学生物传感器,聚焦血糖监测技术突破

ROBOT之鼻 电化学气体传感器静电浪涌防护方案

中科曙光携手中山大学附属第一医院打造精准医学高性能计算平台
洲明数字文化科技与中山大学旅游学院达成战略合作
紫光同创携手中山大学助力集成电路产业创新人才培养
广州医科大学:研发基于金和MXene纳米复合材料的电化学POCT传感器




 中山大学:研究一种无标记电化学生物传感器,无创家庭监测病毒
中山大学:研究一种无标记电化学生物传感器,无创家庭监测病毒





评论