实时生化监测在个性化医疗与疾病诊断中至关重要。纤维电化学传感器因微型化和生物相容性优势,成为可穿戴设备的理想载体。然而,传统表面功能化制备策略导致两大瓶颈:一是活性材料易从高曲率纤维表面剥离,在动态生物环境中(如组织形变、体液浸泡)出现机械退化,导致监测失效;二是涂层均匀性难以控制,批次性能差异高达80%,阻碍规模化应用。
复旦大学彭慧胜院士、孙雪梅副教授团队开发了一种通用共挤出策略,通过将活性材料与导电聚合物PEDOT:PSS悬浮液共挤出,实现柔性纤维电化学传感器的连续化制备。该技术使活性材料均匀嵌入互穿导电聚合物网络,形成稳定界面结构。所得传感器在复杂生物环境中表现出卓越的稳定性与一致性(性能偏差<5%),成功应用于小鼠皮下过氧化氢(H₂O₂)动态监测及脑内抗坏血酸(AA)长达14天的连续追踪

图1揭示了共挤出纤维传感器(EFS)的革新性结构。传统涂层传感器(图1a-i)的活性材料易因弯曲或摩擦脱落,而EFS(图1a-ii)通过活性材料与聚合物网络的均匀融合,从根源解决结构失稳问题。制备流程(图1b)显示:将活性材料(如MnO₂纳米颗粒)、PEDOT:PSS、二甲基亚砜(DMSO)及十二烷基苯磺酸(DBSA)混合挤出至硅胶管,经自发凝胶化、水洗和干燥,形成直径42.31±0.52 μm的连续纤维(图1c)。50组EFS的直径与弯曲刚度偏差均<5%(图1d),SEM图像(图1f-g)和锰元素分布图(图1h)证实活性材料在纤维截面均匀分散,构建了稳定的多孔电化学活性界面。
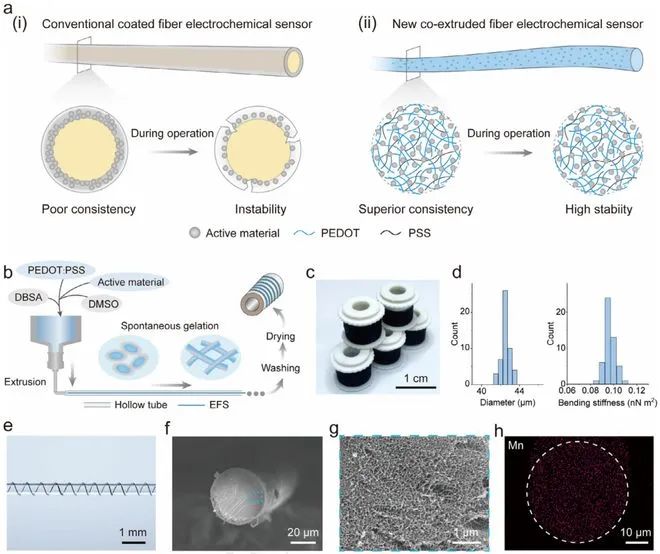
图1:共挤出纤维传感器(EFS)的制备与结构 a) 传统涂层纤维传感器(i)与EFS(ii)示意图。EFS将活性材料均匀嵌入导电聚合物网络,在复杂环境中具有卓越稳定性。 b) EFS制备流程:将含DBSA的PEDOT:PSS溶液与DMSO、活性材料混合后挤入硅胶管,经自发凝胶化、洗涤和干燥成型。 c) 连续生产的EFS卷轴照片。 d) 50个EFS-H₂O₂的直径(左)和弯曲刚度(右)分布。 e) EFS缠绕在毛细管表面的柔性展示。 f,g) EFS-H₂O₂截面的扫描电镜图像。 h) EFS-H₂O₂截面锰元素的均匀分布能谱图。
图2验证了EFS的卓越性能。以过氧化氢传感器(EFS-H₂O₂)为例,其电化学活性面积(10.03 cm²/cm²)远超涂层传感器(1.24 cm²/cm²)(图2a)。在-0.4 V电压下,对1 mM H₂O₂的响应电流达87.57 μA/cm²,灵敏度提升近10倍(图2b-c)。50组EFS灵敏度偏差仅4.9%(图2e),远优于涂层传感器的80%(图2f)。经1000次弯曲(半径2.5 mm)和摩擦循环后,灵敏度衰减<10%(图2g-j),且在PBS中浸泡14天性能无显著下降(图2k-l),凸显其机械与环境稳定性。
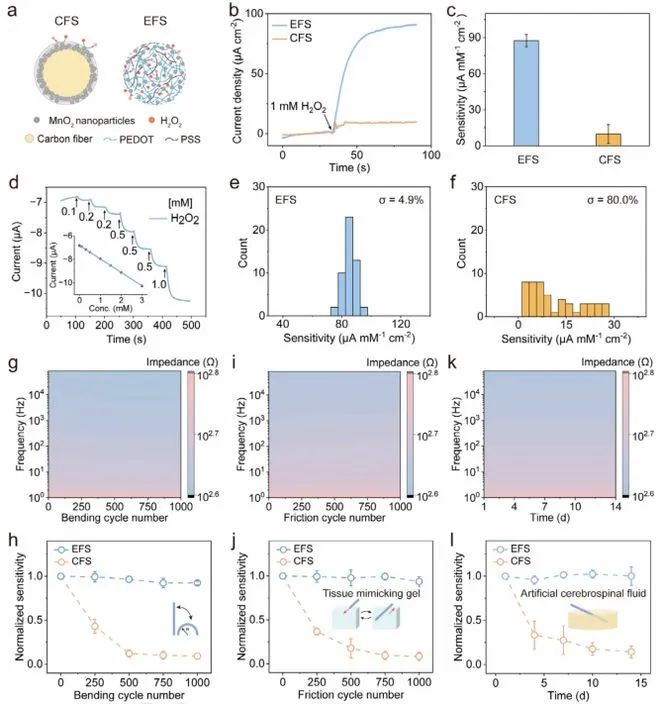
图2:EFS的电化学传感性能、一致性与稳定性 a) 涂层碳纤维H₂O₂传感器(CFS-H₂O₂)与EFS-H₂O₂结构对比。 b) CFS-H₂O₂和EFS-H₂O₂对同浓度H₂O₂的电流响应。 c) 两种传感器的灵敏度对比(n=50)。 d) EFS-H₂O₂的阶梯电流响应(插图为电流随H₂O₂浓度变化)。 e,f) 50个EFS(e)与CFS(f)的灵敏度分布。 g,h) 弯曲1000次后EFS-H₂O₂的阻抗(g)及灵敏度变化(h)。 i,j) 摩擦1000次后阻抗(i)与灵敏度变化(j)。 k,l) PBS浸泡14天中的阻抗(k)与灵敏度变化(l)。
图3展示了技术的普适性。通过更换活性材料,团队成功制备抗坏血酸传感器(EFS-AA,图3a)与葡萄糖传感器(EFS-Glucose,图3d)。EFS-AA对AA的线性检测范围为1-600 μM(图3b),选择性排除神经递质干扰(图3c);EFS-Glucose在0.1 M NaOH中对葡萄糖灵敏度达198.80 μA/mM/cm²(图3e),经Nafion修饰后有效抵抗抗坏血酸和尿酸干扰(图3f)。二者在动态形变和长期浸泡中均保持性能稳定(图3g-i)。
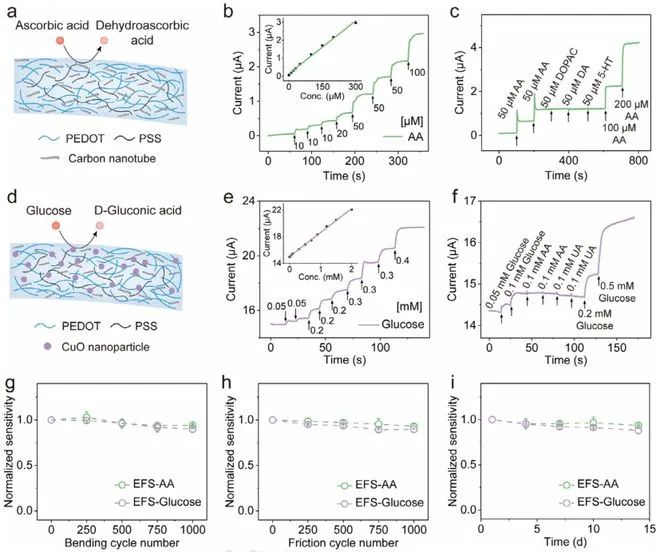
图3:共挤出策略的普适性 a) EFS抗坏血酸传感器(EFS-AA)结构示意图。 b) EFS-AA的电流响应(插图为电流随AA浓度变化)。 c) EFS-AA的抗干扰性能测试。 d) EFS葡萄糖传感器(EFS-Glucose)结构示意图。 e) EFS-Glucose的电流响应(插图为电流随葡萄糖浓度变化)。 f) EFS-Glucose的抗干扰性能测试。 g-i) EFS-AA和EFS-Glucose经弯曲(g)、摩擦(h)及浸泡(i)后的灵敏度保持率。
图4证实了活体应用潜力。EFS植入小鼠皮下7天后,周围组织无炎症反应(图4a-b),实现皮下H₂O₂动态监测(图4c),并在按压、弯曲和摩擦干扰下保持信号稳定(图4d)。更突破性的是,植入大脑的EFS-AA连续工作14天,对抗坏血酸的响应电流振幅无衰减(图4e-g),为慢性神经疾病研究提供新工具。
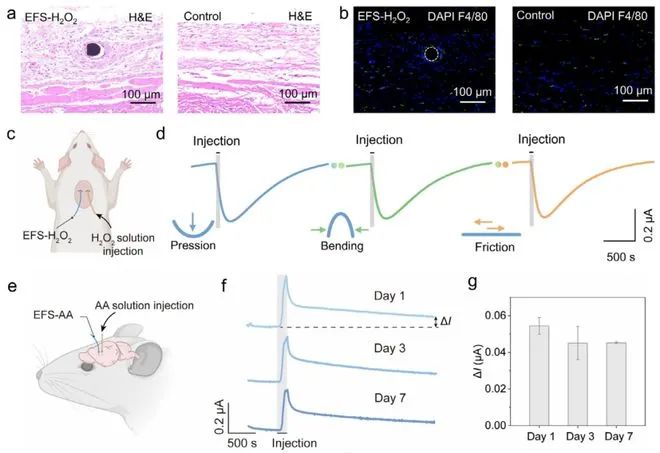
图4:EFS的体内生化物质长期监测 a,b) 小鼠皮下植入EFS-H₂O₂一周后的H&E染色(a)和免疫组化染色(b),蓝色(DAPI)标记细胞核,绿色(F4/80)标记巨噬细胞。 c) 皮下H₂O₂监测示意图。 d) 动态变形下实时监测H₂O₂的稳定性(左:按压;中:弯曲;右:摩擦)。 e) 脑内AA双半球监测示意图。 f) 植入7天内AA实时监测曲线。 g) 植入后7天EFS-AA对AA注射的电流响应变化。
前景展望
该共挤出策略为高性能纤维电化学传感器的规模化生产开辟了新路径。未来通过活性材料拓展与多纤维集成,有望实现单根纤维的多功能监测,推动可穿戴医疗设备在健康管理与慢性病研究中的落地应用。
来源:高分子科学前沿
-
复旦大学
+关注
关注
0文章
20浏览量
8843 -
可穿戴医疗设备
+关注
关注
0文章
13浏览量
15617 -
柔性传感器
+关注
关注
1文章
125浏览量
4898
发布评论请先 登录
复旦大学开源鸿蒙技术俱乐部成立仪式暨智能软件系统技术论坛圆满举办

突破低压传感瓶颈!DLC系列紧凑型高分辨率传感器,让精密测量更简单

厦门大学:高熵合金纳米纤维打造温度免疫的柔性传感器

SGS与复旦大学达成战略合作 携手打造半导体微环境实验室

复旦微电子集团携手复旦大学FPGA创新团队推动产教融合
SICK传感器线缆现场信号稳定性实践与线缆工程指南

Neway微波的稳定性优势
电容式液位传感器的精度与稳定性:技术解析与场景表现
高精度压力测量器:国产万分级精度零点稳定性和满量程稳定性能应用场景分析
复旦大学探索开源人才发展新模式
东华大学:研究基于石墨烯纤维的高性能压力传感器,具有双边致密结构,用于人体运动监测
德国哥廷根大学:研发木质素/ZnO“呼吸纤维”:自供能气流传感的柔性新突破




 复旦大学:开发共挤出技术,突破柔性纤维传感器稳定性瓶颈
复旦大学:开发共挤出技术,突破柔性纤维传感器稳定性瓶颈




评论