研究背景
作为最先进、最便携的储能装置,锂离子电池(LIBs)推动了电动汽车(EVs)的快速发展。然而,当前电动汽车的一个主要缺点是充电慢。为此,美国能源部提出了“极速充电”(XFC)的目标,要求充电时间缩短为15分钟(4C)。到目前为止,使用石墨负极和碳酸亚乙酯(EC)基电解质的商业LIB无法实现极速充电,因为在高倍率下,石墨的工作电位很容易降至0 V,导致负极析锂。因此,需要改善Li+在电解质中的传输动力学,从而实现石墨负极的极速充电,同时避免锂金属的沉积。
成果简介
近日,浙江大学范修林教授,马里兰大学王春生教授和中国科学院物理研究所王雪锋研究员在Advanced Materials上发表了题为“50C fast-charge Li-ion batteries using graphite anode”的论文。该论文设计了一种新型电解质,可以在避免析锂的情况下,对微尺寸石墨负极进行极速充电。实验表征和模拟表明,高离子电导率、低锂离子去溶剂化能和具有保护作用的SEI对极速充电至关重要。
根据该标准,设计了两种快速充电电解质:1.8 M LiFSI in DOL和1.0 M LiPF6 in FEC/AN(体积比为7:3)。在50C时,前一种电解质使石墨电极容量达到180 mAh g-1,是传统电解质的10倍。在4C充电和0.3C放电条件下,后一种电解质使LiNi0.8Co0.1Mn0.1O2||石墨电池提供高达170 mAh g-1的可逆容量。
研究亮点
(1)本工作证明了降低Li+在电解质中的去溶剂化能有望实现快速的界面动力学,而提高电解质的离子电导率和形成薄而坚固的SEI可以实现具有良好循环稳定性的超高倍率石墨负极。
(2)理论计算和实验结果表明,1.8 M LiFSI in DOL电解液使微尺寸天然石墨(NG)电极在20C下实现了315 mAh g-1的容量,且没有衰减。即使在50C 下,仍保持180 mAh g-1的高可逆容量。在-30℃下,可逆容量为310 mAh g-1。
图文导读
储能速率取决于Li+在正负极之间的迁移速度。原则上,Li+在充电过程中经历三个步骤(图1a):(a)溶剂化Li+在体电解质中的扩散,(b)Li+去溶剂化,(c)Li+穿过SEI。溶剂的物理化学性质和浓度决定了Li+的扩散率,而Li+内溶剂化壳的成分影响SEI的组成,从而决定SEI中的Li+传输动力学。加速Li+传输将显著增强电化学动力学,这需要具有高离子电导率(IC)、低去溶剂化能(ΔEdsv)和低Li+迁移能垒(ΔESEI)和小的面积比电阻(ASR)。
为了设计具有这些特性的电解质,首先通过实验和DFT计算测量常用盐和溶剂的离子电导率(图1b)、ΔEdsv(图1c)和还原电位(Gred,图1d)。根据结果,FSI-在阴离子中表现出最低的ΔEdsv(图1c)和最高的还原电位(图1d),表明FSI-可以实现低的去溶剂化能垒和富含无机物的SEI。
对于溶剂,AN基电解质表现出优异的离子电导率,可增强电解质内的Li+迁移和传输(图1b),而与Li+相互作用最弱的DOL溶剂(图1c)有望改善去溶剂化动力学。FEC溶剂有利于构建富含LiF的SEI,因为它可以在1.0 V左右促进LiF的形成。富含LiF的SEI非常薄并且具有低ASR,因为LiF具有高离子电导率和低电子电导率。
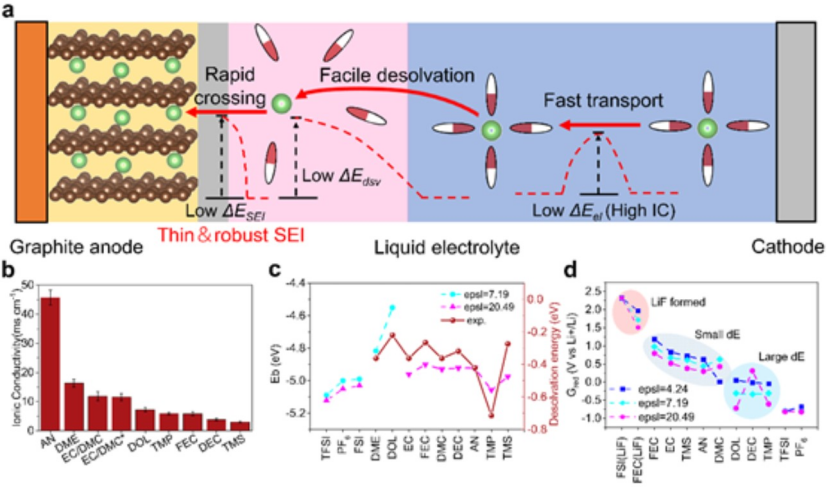
图 1、a)石墨负极快充示意图。b)在不同溶剂中1.0 M LiFSI的离子电导率。c)量子化学计算的结合能和测量的去溶剂化能。d)计算出的阴离子和溶剂的还原电位。
选择LiFSI作为盐,因为它在所盐中具有最好的解离性,且最容易形成LiF(图1d),而DOL具有最低的ΔEdsv(图1c),因此作为溶剂。为了最大化倍率性能,制备了1.8 M LiFSI DOL电解液。使用NG||Li半电池评估了不同电解质中微尺寸天然石墨(2.5NG)的倍率性能。
碳酸盐电解液中NG从1C开始,容量快速下降,而即使在20C和50C下,1.8M LiFSI DOL电解液中的NG负极也能够分别提供315和180 mAh g-1的容量(图2a)。图2b显示,由于形成了LiCx,对于1.8 M LiFSI DOL,在1C时出现三个低于 ~0.2 V的电压平台。即使倍率增加到20C,电池仍有明显的电压平台。
由于倍率性能是在双电极电池中测量的,因此总过电势由两部分组成:石墨负极和锂金属电极的过电势。石墨负极的真实过电势(图2c)是通过从上述充放电曲线的总过电势中减去恒流锂电镀/剥离测试中的锂金属过电势获得的。当倍率从1C增加到50C时,石墨电极在1.8 M LiFSI DOL电解质中的过电势为0.032至0.153 V,远低于碳酸盐电解质(从0.037至0.335 V)(图2c)。
采用高倍率(10C)的锂化电流进行恒流间歇滴定技术(GITT),以了解石墨电极/LiCx的锂化/脱锂过电位。在锂化过程中,具有1.8 M FSI DOL电解质的电池容量大于360 mAh g-1,而具有商用碳酸盐电解质电池的容量为80 mAh g-1(图2d)。商用碳酸盐电解质(142 mV)的整体电位上升幅度是1.8 M LiFSI DOL电解质(31 mV)的4.6倍。
根据Nyquist图的拟合结果,电池电阻主要由体电阻(Rb)、表面层电阻(Rsei)和电荷转移电阻(Rct)组成(图2e)。1.8 M LiFSI DOL电解质中的Rsei和Rct值(9.1和4.7 Ω)远低于碳酸盐电解质中的值(33.2和15.1 Ω),表明1.8 M LiFSI DOL电解质中具有更快的界面反应动力学。
图2f显示,采用碳酸盐电解质的NG||Li半电池在20C下只有40 mAh g-1的容量,而采用1.8 M LiFSI DOL电解质的电池具有315 mAh g-1的高可逆容量。在高电流密度下,锂金属电极必须每1000次循环更换一次,以消除有害影响。
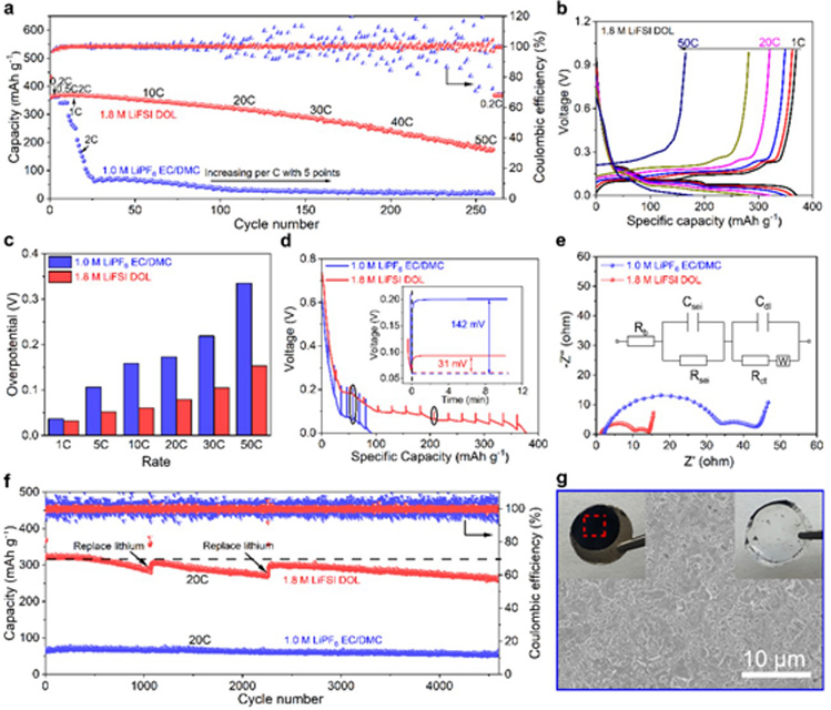
图 2、a)具有1.8 M LiFSI DOL和1.0 M LiPF6EC/DMC(体积比为1:1)的NG||Li电池倍率性能。b)具有1.8 M LiFSI DOL的NG||Li电池充放电曲线。c)两种电解质中不同倍率下石墨电极过电位的演变。d)在10C下,NG||Li电池通过GITT测量得到的放电电压曲线。具有两种电解质的NG||Li电池e)阻抗谱和f)在20C下的长循环性能。g)1100次循环后,锂金属电极的表面SEM图像。
进行X射线光电子能谱(XPS)以确定循环石墨电极上的SEI化学成分。对于在碳酸盐电解质中形成的SEI(图3a),在C 1s光谱中检测到有机(RCH2OLi,290.7 eV)和无机(Li2CO3,291.2 eV)成分。用Ar+溅射120秒后,SEI层的成分主要由碳物种(~80%)组成(图3b),表明大部分SEI成分来自EC分解。
同时,溅射过程中Li2CO3和其他无机物质(O、C、P)的信号相对较弱,表明在碳酸盐电解质中形成的SEI富含有机物。
与源自碳酸盐电解质的SEI不同,1.8 M LiFSI DOL电解质中的NG的SEI包含更多的无机(LiO、LiF)物质(图3c、d)。F 1s光谱中强的LiF(685.9 eV)信号和高的F含量比例证实,SEI中富含LiF。与富含有机物的SEI相比,富含LiF的SEI能够实现更快的动力学,因为LiF具有宽的带隙和高的化学/电化学稳定性,从而阻止副反应。
图3e通过从头算分子动力学(AIMD)模拟了石墨上的原子SEI结构。对于碳酸盐电解质,可以发现开环的EC、LixPF6和Li2CO3簇,表明SEI主要是由EC溶剂的分解产生。对于1.8 M LiFSI DOL电解液,LiF和LiNxSyOz簇在界面处形成,而没有DOL分解产物,表明LiFSI在界面处更容易分解。石墨上形成的LiF有效地阻止了电解质的连续反应,从而提高了库仑效率。
采用低温透射电子显微镜(cryo-TEM)技术,可以保留SEI的原始形貌,分析SEI薄膜的具体结构。图3f,j显示,对于碳酸盐电解质,生成的SEI呈现经典的马赛克结构,纳米级Li2CO3和 Li2O 颗粒(图3g)分散在无定形有机成分中。然而,在1.8 M LiFSI DOL电解液中生成的SEI主要的无机成分是尺寸为5-10 nm的LiF和Li2O(图3j,k)。
与在碳酸盐电解质中形成的厚度> 40 nm的SEI不同(图3g),在1.8 M LiFSI DOL电解质中衍生的SEI仅为15 nm(图3k),这有利于Li+穿过SEI进行快速传输。
能量色散X射线光谱(EDX)的相对含量分析表明,在1.8 M LiFSI DOL电解液中形成的界面相中无机物比在碳酸盐电解液中形成的界面相多十倍以上(图3l)。ADF STEM和EELS也对1.8 M LiFSI DOL电解质中形成的界面相进行了分析,结果表明元素在石墨边缘富集(图3m),而碳酸盐电解质中的元素分布广泛(图3i)。
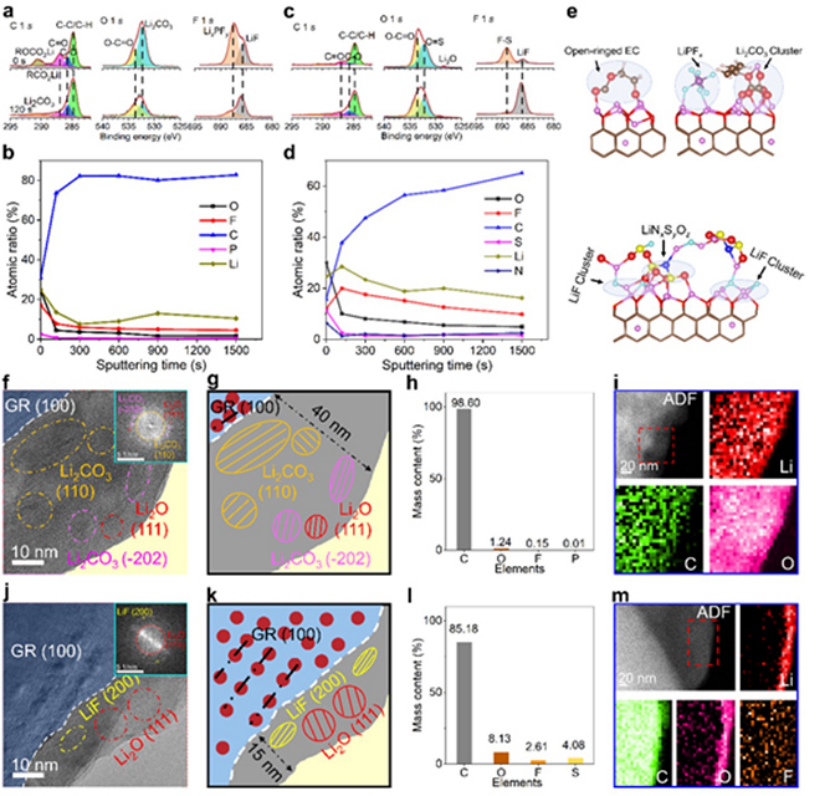
图 3、在a)碳酸盐电解质和b)1.8 M LiFSI DOL中,石墨电极上SEI被Ar+溅射0 s和120 s后的C 1s、O 1s和F 1s光谱。在b)碳酸盐电解质和d)1.8 M LiFSI DOL中循环的石墨负极上SEI的元素含量。e)AIMD模拟了石墨和电解质之间的原子SEI结构。
在f)碳酸盐电解质和j)1.8 M LiFSI DOL电解质中形成的SEI薄膜的高分辨率低温TEM图像。g,k)两个高分辨率低温TEM图像的相应示意图。在h)碳酸盐电解质和l)1.8 M LiFSI DOL电解质中形成的SEI膜的不同元素含量。i)碳酸盐电解质和m)1.8 M LiFSI DOL电解质中石墨表面的高分辨率ADF STEM和EELS结果。
使用具有高载量的微尺寸天然石墨负极和LiFePO4正极评估了1.8 M LiFSI DOL对锂离子电池超快充电能力的影响。首先评估了在不同充电倍率下,2 mAh cm-2石墨电极的循环稳定性。在如此高的载量下,1.8 M LiFSI DOL电解质使石墨电极在4C时的容量为320 mAh g-1,在10 C时的容量为150 mAh g-1(图4a),而碳酸盐电解质在4C时仅为20 mAh g-1(图4a)。
此外,还评估了电池的低温性能。图4b,c的低温测试显示,随着温度从25℃逐渐降低到-30 ℃,1.8 M LiFSI DOL在-30 ℃下仍有300 mAh g-1的容量,而碳酸盐电解液-30℃下几乎没有容量。在60C下,具有1.8 M LiFSI DOL电解质的软包LFP||NG电池容量为60 mAh g-1,在长循环过程中没有衰减,库仑效率稳定为99.99%(图4d),远远超过了使用碳酸盐电解质的电池性能。
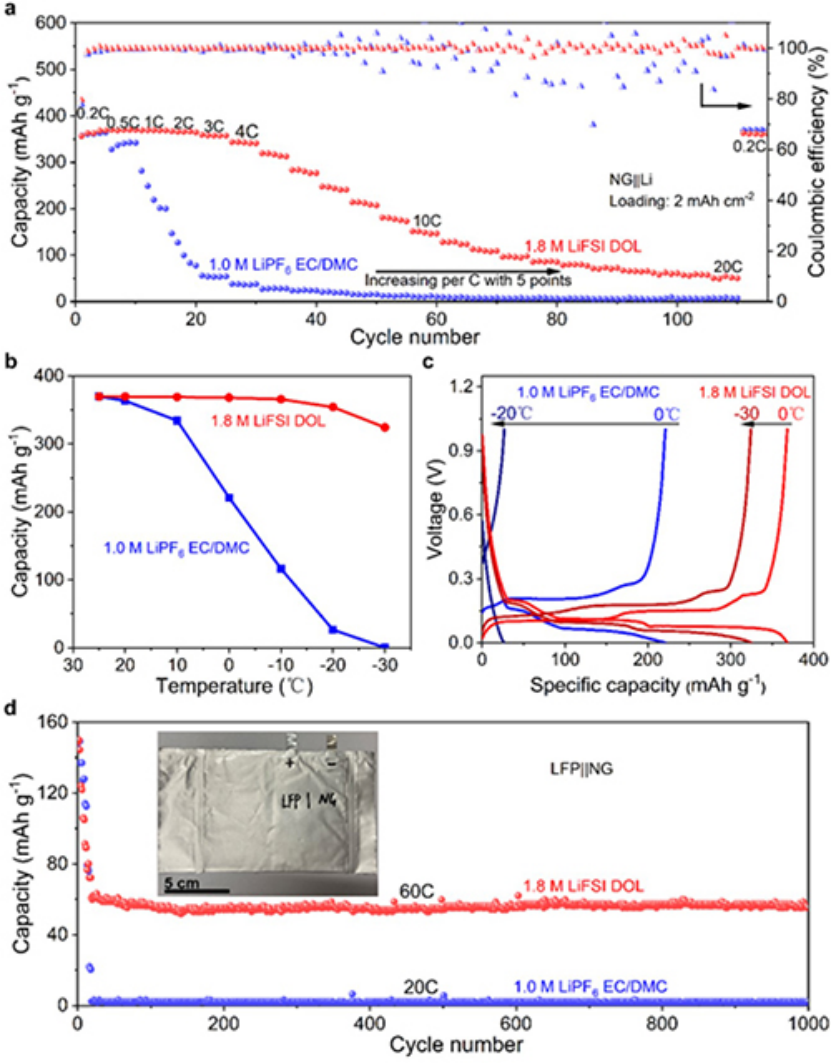
图 4、具有两种电解质的NG||Li电池 a)倍率性能,b)低温性能和c)相应的充放电曲线。d)具有两种电解质的LFP||NG软包电池长循环性能。
为了与高压LiNi0.8Mn0.1Co0.1O2(NCM811)正极相匹配,还配制了1.0 M LiPF6FEC/AN高压快速充电电解质。1.0 M LiPF6 FEC/AN中具有和不具有阴离子的典型Li+溶剂化结构如图5a、b所示。RDF结果表明,Li+的初级溶剂化结构为Li(PF6)(FEC)3AN。溶剂化壳中的FEC溶剂和PF6-阴离子倾向于在界面处被还原形成LiF,而AN溶剂加速了电解质内的锂离子传输。
在20C时,1.0 M LiPF6 FEC/AN电解质使石墨电极能够实现230 mAh g-1的高容量,优于碳酸盐电解质(40 mAh g-1)(图5c)。此外,具有1.0 M LiPF6/FEC:AN的NCM811||NG电池,在恶劣的循环条件下(4C充电0.3C放电)依然能够保持170 mAh g-1的高可逆容量。
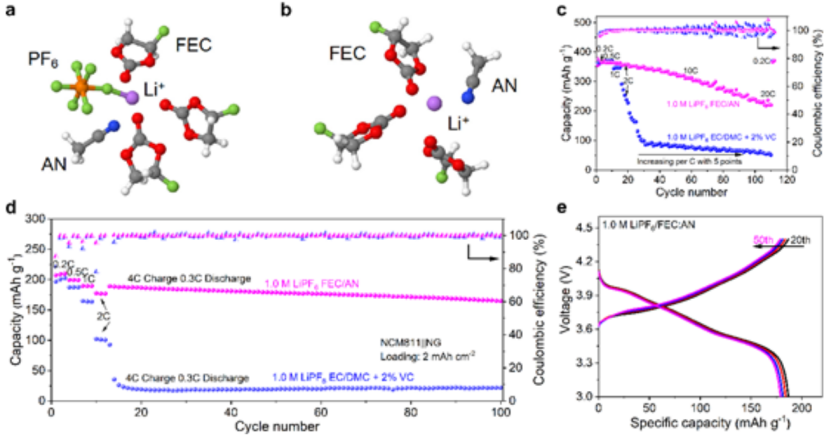
图 5、在a)有阴离子和b)没有阴离子情况下,1.0 M LiPF6FEC/AN电解质的典型Li+溶剂化结构。NG||Li电池的c)倍率性能、d)长循环性能,以及e)在恶劣条件下,具有1.0 M LiPF6FEC/AN的NCM811||NG电池充放电曲线。
总结与展望
极速充电的锂电池需要对电解质进行优化,电解质的优化标准包括:低的Li+去溶剂化能,高离子电导率,以及在石墨表面形成薄而坚固的SEI。根据该标准制备了1.8 M LiFSI DOL和1.0 M LiPF6FEC/AN(体积比7:3)两种快速充电电解质。前者使石墨电极在20C和50C时分别达到315 mAh g−1和180 mAh g−1的极高容量。
XPS和低温TEM表征表明,石墨电极表面存在均匀且富含LiF的SEI。载量为~2 mAh cm−2的NG||Li电池在-30℃下具有320 mAh g-1的高容量。LFP||NG电池在20C时容量为80 mAh g-1,软包电池在60C下容量为60 mAh g-1。本研究提供了一种简单可行的电解质设计原则,有望实现石墨基锂电池的快速充电。
审核编辑:刘清
