阳极表面材料 - 究竟是什么限制了电池的容量?
2014年05月05日 09:50 来源:知乎 作者:陈远威 我要评论(0)
三:电池的大问题之二,阳极表面材料
大家好,我又回来了。
如果你能坚持每行读下来一直读到这里,恭喜,你对电池的理解已经上了一个层次。
现在回顾上一部分的内容。啥么??全忘了??不就一句话么?由于不做功但是必不可少的电解质以及其他辅助材料的存在,电池的能量密度被稀释了。
这些额外重量到底有多少??
电解质的重量一般占电池全重15%(链接找不到了)隔膜没查到。估计把外壳,外接电极之类的辅助材料都算上,总重应该不超过电池总重的50%。
不对啊,电池虽然掺‘水’了,但也不至于水得如此啊。市面上的锂离子电池们的能量密度也就单质锂的1%左右。这到底又发生了什么?(这句式为何这么熟悉呢?)
喝点鲜橙多,让我们看看最常见的钴酸锂电池(Tesla Roadster)的电化学反应式。
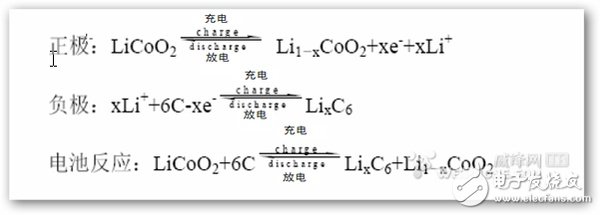
醒醒啊!!化学不好没关系,不要晕倒啊!!都读到这里了,你也知道达主会归纳的呀!!
发生电子转移的其实只是一部分锂与钴,其它的元素均不参与电子转移。
![]() 然后我们做个小计算:单质锂的原子量为6.9,能贡献1个电子参与电子转移。氧化剂来自空气,不需要考虑。
然后我们做个小计算:单质锂的原子量为6.9,能贡献1个电子参与电子转移。氧化剂来自空气,不需要考虑。
钴酸锂电池的电池反应的反应物总分子量为98+72=170,但只能贡献半个电子参与电子转移。因为只有部分锂原子会发生反应。
假如我们认为这两个电子的做功是一致的,那么就可以估计一下这两种能量载体的能量密度之比了。
电池能量密度:燃料能量密度=(0.5 /170) /(1/6.9) =2.03% 电池完败。
考虑到电池有一半重量是辅助材料,我刚才没算进去。于是还得打个折。就剩下1%了。
所以能量密度就成了这样:锂 43.1MJ/Kg 锂离子电池0.36~0.875MJ/Kg
呵呵呵呵呵呵呵……还跟得上么??四则运算多简单呀。现在知道发生了什么了吧??
现在你们是否明白 我为啥说:电池背后的化学限制了电池的能量密度。
接下来我们的问题是:为什么电池的化学反应要那么复杂,直接降低了电池的能量密度。
这个问题展开说会比较复杂,估计大部分人没耐心看完。所以先给个简单答案:
为了有序。
好了,没耐心的人,你们可以走了。下面真的很长,能读完的都不是一般人。
开始长篇之前再放张图:
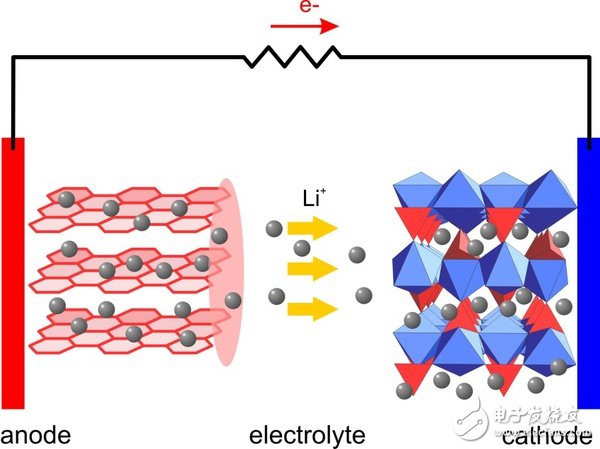
剩下的同学们,是不是觉得这图很熟悉?其实还是锂电池的示意图,只是这回因阴极阳极的表面结构都显示出来了。大家有没有觉得它们都很整齐规矩啊??
整齐规矩换个说法,有序。
为什么阴极阳极的表面结构都需要有序?因为要保证在充电/放电时,氧化还原反应只在阴极和阳极的表面发生,这样才能有电流。
我们先看石墨(C6)所在的阳极。
阳极的任务很简单,放电时保证锂原子(不是离子)都在阳极表面失去电子,充电时再把它们抓回来就好了。由于充电时阳极电压低,带正电的锂离子会自发向阳极移动,得到电子回归为锂原子。
似乎没有石墨什么事情啊??
如果是一次性电池,确实不需要石墨。但如果是可充放电池,阳极表面材料不是石墨也会是其它物质。
别卖关子了,快说到底咋回事??
急啥。这得仔细想想。充电时,锂离子会在阳极表面得到电子成为锂原子。然后呢??
我们都知道 所有金属都是良好电子导体,锂是金属,所以锂是良好电子导体。于是先到阳极的锂原子成为了阳极的一部分,于是后到阳极的锂离子加入了前锂的行列。。。。
于是完全由锂原子构成的晶体出现了。这个过程,又称析晶。结果是锂晶体会刺穿隔膜到达阴极,于是电池短路报废了。
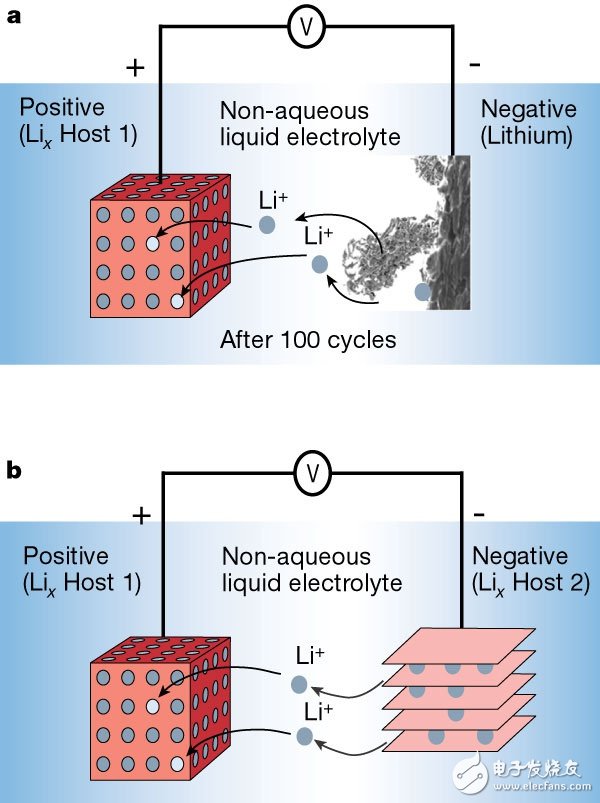
对于析晶这一现象,我们可以这么理解。
在充电过程中,我们对于锂离子的控制实际上很弱。我们只能保证锂离子会移动到阳极表面,但我们无法保证锂离子会均匀地分布在阳极表面。因此在没有外来约束条件下,充电时锂晶体会在阳极表面无序生长,形成枝晶 (dendritic crystal)。
所以一定要有个约束条件。要挖个坑让锂离子往里面跳。
这个坑的具体表现即为阳极表面的石墨材料。如上图所示,石墨层之间的空隙够大,足以容纳单个锂原子,但也只能容纳单个锂原子;然后石墨层与锂原子之间的物理吸附作用可以稳住锂原子,于是锂原子在没有外来电压时候也能安心待在阳极表面。
如此以来,锂原子便不会野蛮生长了。但能量密度也上不去了。
本文导航
- 第 1 页:究竟是什么限制了电池的容量?
- 第 2 页:阳极表面材料
- 第 3 页:阴极表面材料




用户评论
查看全部 条评论
查看全部 条评论>>